Disocirano sazrijevanje horionskih resica. Patologija posteljice
Patološka slika placente kod FPI karakteriše prvenstveno degenerativno-distrofične promene, oštećena BMD, promene u permeabilnosti strome vila, znaci poremećenog sazrevanja vile i niz drugih pojava. U ovom slučaju, težina patoloških promjena ovisi o težini i trajanju tijeka komplikacija i prirodi kompenzatorno-prilagodljivih reakcija.
Često je razvoj FPN-a praćen smanjenjem parametara posteljice (težina, volumen, površina majke), što ukazuje na kršenje njegovih kompenzacijskih sposobnosti. Smanjenje mase placente prvenstveno je posljedica kršenja njene funkcije stvaranja proteina. Češće nego normalno, postoji ekscentrični ili omotač pupčane vrpce. Količina Whartonovog mliječa u pupčanoj vrpci se smanjuje, elastičnost pupčane vrpce se gubi, zidovi njezinih žila su zbijeni, pronalaze se lažni čvorovi, koji su proširene vene.
Među patomorfološkim promjenama koje se javljaju u posteljici u FPN-u su infarkt, fibrinoidne naslage iz interviloznog prostora, fibrinoidna degeneracija epitela resica, strome i vaskularnih zidova, kolagenizacija strome, smanjenje broja krvnih žila u stabljika i terminalne resice, bubreg smanjenja volumena simpatikusa sa znacima distrofije, morfološka nezrelost posteljice, dominacija intermedijarnih resica i disocirani razvoj kotiledona.
Nastanak infarkta u placenti prvenstveno je posljedica vaskularne tromboze resica i horionske ploče, praćene stromalnom ishemijom i taloženjem fibrinoida. Proporcionalno težini FPN-a, broj terminalnih resica se smanjuje, otkrivaju se njihova hipoplazija, nepravilna lokacija u interviloznom prostoru, konglomeracija i fibrinoidni omotač. Istovremeno se smanjuje površina lumena kapilara resica, njihov volumen i broj.
U epitelu intermedijarnih resica otkrivaju se distrofične promjene. Područja deskvamacije i stanjivanja epitela izmjenjuju se s područjima hiperplazije i formiranih sincicijskih čvorova, koji su nakupine jezgara sincitiotrofoblasta. Kako se težina FPI povećava, proporcionalno se povećava i broj nezrelih resica. Uz izražen FPN u stromi terminalnih resica, uz edem, nalaze se procesi fokalne fibrinoidne nekroze. Povećava se broj skleroziranih terminalnih resica.
Kapilarna tromboza ukazuje na poremećaje cirkulacije koji se javljaju u FPI. Tu su i krvarenja, edem strome resica, srčani udari, međuvilozni trombi.
U slučaju kršenja BMD-a, nalaze se promjene u krvnim žilama koje karakterizira oticanje endotelnih stanica kapilara, arterija i venula. U žilama matičnih resica uočena je koncentrična proliferacija s odvajanjem endotelnih stanica. U zidovima arterija otkrivaju se izražene distrofične promjene, otok, disocijacija struktura, fokalna proliferacija endotelnih stanica, što dovodi do stenoze lumena. S teškim FPI oko zidova arterija i arteriola, limfocitna infiltracija se nalazi u resicama stabljike, obično praćena vazokonstrikcijom.
Zbog stagnacije krvi, povećanog taloženja fibrinoida, stvaranja petrifikacije i infarkta vila, smanjuje se volumen međuviloznog prostora, što dovodi do kršenja hemodinamike. Sa povećanjem težine FPN-a, stanice citotrofoblasta prolaze kroz teške distrofične promjene (liza, destrukcija citoplazmatskih i nuklearnih membrana, edem i fibrinoidna degeneracija).
Patomorfološki poremećaji koji se javljaju usko su povezani s promjenama u funkcijama posteljice.
Smanjenje transportne funkcije placente u FPI posljedica je smanjenja njene vaskularizacije, velikog raspršenja krvnih žila, kao i smanjenja njihovog specifičnog volumena i površine žila terminalnih resica.
Supresiju izmjene plinova prati smanjenje broja sincitiokapilarnih membrana.
Stanje horijalnog epitela i funkcionalno aktivnih simplastičnih bubrega morfološki je ekvivalent intenzitetu metabolizma u placenti i transportu metabolita preko placentne barijere. Ovisno o težini FPN-a, broj resica sa simplastičnim bubrezima smanjuje se za 1,5-4 puta.
Jedna od najvažnijih strukturnih komponenti koja odražava hormonsku funkciju placente je trofoblast. Sa povećanjem težine FPN-a, smanjuje se specifični volumen citotrofoblasta.
Barijernu funkciju posteljice osigurava širok sloj korionskog epitela, centralna lokacija krvnih žila u resicama i intersticijsko tkivo. U zavisnosti od težine FPI u posteljici, povećava se broj horionskih resica sa fibrinoidom. Prekomjerno taloženje fibrinoida na površini resica i u stromi viloznog horiona smanjuje njihovu aktivnu površinu, što stvara nepovoljne uslove za ishranu i izmjenu plinova fetusa.
Uprkos involutivno-distrofičnim i cirkulatornim poremećajima u placenti, koji se razvijaju u FPN, paralelno se manifestuju i zaštitne i adaptivne promjene koje uključuju hiperplaziju terminalnih resica i kapilara; povećanje njihovog broja, proširenje lumena, pomicanje kapilara na bazalnu membranu, stvaranje i povećanje sincitiokapilarnih membrana, povećanje broja sincicijskih bubrega, što dovodi do povećanja površine izmjene između krvotoka majke i fetusa. Kompenzacijske reakcije trofoblasta očituju se proliferacijom korionskog epitela, što osigurava povećanje korisne površine plodnog dijela posteljice.
U vezi s isključenjem određenog dijela placente iz krvotoka kod poremećaja cirkulacije, povećava se broj malih terminalnih resica i citotrofoblastnih elemenata kao adaptivni odgovor.
Kompenzacijske reakcije uočene u mikrovaskulaturi i korionskom epitelu kod FPI su nespecifične prirode i provode se korištenjem mehanizama razvijenih u toku evolucije i ontogeneze. Placenta je višenamjenski organ čija morfološka struktura osigurava obavljanje različitih funkcija istim strukturama. Zbog ove osobine, s razvojem kompenzatorno-prilagodljivih reakcija, povećanje djelotvornosti jedne funkcije može dovesti do smanjenja djelotvornosti druge.
Ostvarenje kompenzatorno-prilagodljivih reakcija na tkivnom nivou otežava i poremećaj sazrevanja horiona. Istovremeno, na pozadini zrelih terminalnih resica, nalaze se grupe resica s labavom stromom i slabo razvijenom vaskularnom mrežom. Disocirano sazrijevanje resica je tipična morfološka karakteristika hroničnog FPI.
Dekompenzirani oblik FPN je praćen povećanjem broja resica sa subepitelnim rasporedom krvnih žila, što treba smatrati iscrpljivanjem funkcionalnih rezervi fetoplacentarnog kompleksa. U placenti se otkrivaju infarkti, masivne naslage fibrinoida u predjelu bazalne ploče i plodnog dijela posteljice, kolagenizacija strome, sužavanje međuviloznih prostora, povećanje broja sincicijskih nodula sa znacima distrofije.
U ovom slučaju, u pravilu, postoji veliki volumen nefunkcionalnih zona koje se sastoje od zalijepljenih resica, majčinog fibrinoida i kalcifikacija. Često se izraženi hemoragijski poremećaji otkrivaju u obliku krvarenja različite dobi u međuviloznom prostoru. U većini malih krajnjih resica, siromašnih krvnim sudovima, stroma je prožeta gustom mrežom kolagenih vlakana. Odvojene grupe terminalnih resica u blizini bazalne ploče iu plodnom dijelu posteljice okružene su masivnim slojem fibrinoida, dok su neke od njih u stanju nekrobioze i nekroze.
Patološka nezrelost placente uključuje sljedeće opcije.
Varijanta embrionalnih resica- nastaje kao rezultat zaustavljanja razvoja posteljice u ranim fazama embriogeneze i karakterizira ga perzistencija embrionalnih resica u posteljici II-III trimestra trudnoće. Javlja se kod toksikoze trudnica, dijabetes melitusa, nekih zaraznih bolesti majke i fetusa. Makroskopski: posteljica je uvećana, edematozna, lobularna. Mikroskopski: višestruke resice sa labavom stromom, prevladavaju mnoge Kaschenko-Hofbauerove ćelije i stromalni kanali. SCM i sincicijski bubrezi su odsutni, male su avaskularne resice, intervillozni prostor je proširen. U slučaju difuznog širenja embrionalnih resica, trudnoća se najčešće završava ranim spontanim pobačajem. Perzistencija embrionalnih resica u količini od 40-50% svih resica javlja se kod ranih gestoza trudnica, dijabetes melitusa, izoserološke nekompatibilnosti krvi majke i fetusa, nekih specifičnih infekcija (rubeola, sifilis, toksoplazmoza). Tipična kombinacija sa abnormalnostima u obliku placente i vezivanja pupčane vrpce, kao i pobačaja ili pothranjenosti fetusa.
Opcija srednje resice karakterizira prevlast resica promjera 80-110 µm sa malim brojem bočnih, sitnih grana, što ukazuje na prestanak formiranja viloznog stabla u fazi razvoja srednjih resica. U ovom slučaju mogu prevladati srednje zrele ili srednje nezrele resice. Varijanta s dominacijom srednje nezrelih resica je češća kod spontanih pobačaja i antenatalne smrti fetusa. Dominacija srednje zrelih resica je češća kod spontanih pobačaja, kasnih gestoza, višeplodnih trudnoća. Dovoljna vaskularizacija resica omogućava fetusima da dostignu 37 sedmica ili više.
Varijanta skleroziranih haotičnih resica- nastaje u drugom tromjesečju trudnoće kao rezultat dominantnog razvoja strome resica i odsustva njihovog kapilarnog korita. Makroskopski: posteljica je smanjena (hipoplazija). Mikroskopski: preovlađuju male resice sa pojedinačnim uskim kapilarama, njihova stroma je bogata ćelijama, sincicij je slabo izražen, sincicijski pupoljci su odsutni, embrionalnih resica ima malo ili ih nema. Preovlađivanje ove vrste nezrelosti uočava se kod spontanih pobačaja, antenatalne smrti fetusa, teške gestoze i višeplodnih trudnoća. Kod većine njih uočena je izražena hipoplazija placente, hipotrofija fetusa i novorođenčeta. Stopa mortaliteta je 40%. Često fetus umire u 24-25 sedmici, rjeđe na kraju trudnoće, ali dijete se može roditi živo sa malom tjelesnom težinom.
Disocirana razvojna varijanta- najčešća varijanta patološke nezrelosti, javlja se krajem II - početkom III trimestra trudnoće zbog neujednačenog razvoja pojedinačnih kotiledona. Posteljica, zajedno sa zrelim područjima, sadrži grupe ili čitava polja embrionalnih, hipovaskulariziranih resica i područja kompenzatorne kapilarne hiperplazije. Razlozi nisu u potpunosti shvaćeni. Može se primijetiti kod kasnih gestoza trudnica, latentnih oblika dijabetes melitusa. Ako preparati sadrže dovoljan broj zrelih, malih, dobro vaskulariziranih resica, tada se obično rađaju donošena novorođenčad s normalnom težinom ili blagom hipotrofijom.
Vrlo rijetke vrste nezrelosti uključuju horangiosus i obliterirajuća angiopatija... Vrijeme njihovog nastanka je prvo tromjesečje trudnoće. Za horangiosa karakterizira difuzno povećanje broja viloznih kapilara, što se može smatrati primarnom ili sekundarnom (dijabetes melitus) razvojnom anomalijom, često dovodi do perinatalnog mortaliteta. Ishod trudnoće je često nepovoljan, završava se ranim pobačajem ili antenatnom smrću fetusa. At obliterirajuća angiopatijažile stabljike i intermedijarne resice su stenozirane ili obliterirane punjenjem lumena vezivnim tkivom različitog stepena zrelosti. Smatra se da je takva obliteracija posljedica majčinog intenzivnog pušenja ili izloženosti profesionalnim faktorima (proizvodnja boje i sl.). U 30% slučajeva fetus umire u maternici ili se beba rodi prerano.
HISTOLOŠKI PREGLED PLACENTE
USKLAĐENOST PLACENTE SA VRIJEMEM GESTIJENJA (da, ne)
Povreda sazrevanja resica(ne, +, ++, +++):
patološka nezrelost:
varijanta embrionalnih resica, varijanta nezrelih intermedijarnih resica, varijanta zrelih intermedijarnih resica, varijanta haotičnih skleroziranih resica.
relativna nezrelost:
disocirano sazrevanje, prerano sazrevanje resica
2. INVOLUTIVNE DISTROFIČNE PROMJENE (ne, +, ++, +++)
edem (+, ++, +++), fibrinoid (+, ++, +++), fibrin (+, ++, +++), pseudoinfarkt (+, ++, +++), kalcifikacije ( +, ++, +++), tromboza interviloznog prostora (+, ++, +++), distrofične promjene u stromi resica i vaskularnih zidova (+, ++, +++), fibroblastna reakcija ( +, ++ , +++), skleroza vila (+, ++, +++).
3. REAKCIJE KOMPENZATORA (ne, +, ++, +++):
angiomatoza (+, ++, +++), hiperemija (+, ++, +++), sincitio-kapilarne membrane (+, ++, +++) sincicijski bubrezi (+, ++, +++) , povećanje staničnih otočića (+, ++, +++), mala cistična transformacija citotrofoblasta (+, ++, +++)
4. INFEKTIVNE LEZIJE:
horioamnionitis placente (ne, +, ++, +++), parijetalni horioamnionitis (ne, +, ++, +++), parijetalni deciduitis (ne, +, ++, +++), bazalni deciduitis (ne, +, ++, +++), interiluzitis - subhorijski (ne, +, ++, +++) - centralni (ne, +, ++, +++), bazalni (ne, +, ++, + ++); vilusitis (ne, +, ++, +++), umbilikalni flebitis (ne, +, ++, +++), umbilikalni arteritis (ne, +, ++, +++), funikulitis (ne, +, ++), izolovani vaskulitis sudova potpornih resica i horionske ploče (ne, +, ++, +++), marginalni placentitis (ne, +, ++), oticanje vaskularnog endotela resica (arteriole , venule) (ne, +) ... eritroblasti u lumenu krvnih sudova (ne, +);
MORFO-FUNKCIONALNO STANJE POSLE:
Kompenzirano stanje.
("akutni otkaz (ne, +, ++, +++).
bojenje školjki mekonijumom (ma karakteristika obrezivanja); retroplacentarni hematom (m karakteristika obrezivanja) - ("+, ++. +++), parabazalni hematom do jednog dana (+, ++. +++), parabazalni hematom preko dana (+, ++, +++), hematom pupčane vrpce preko jednog dana (+ ), intervillous hematom do jednog dana (+, ++, +++), intervillous hematom duže od jednog dana (+, ++. +++), tromboza pupčane vene (+), vaskularni tromboza resica (+, ++, ++ +), vaskularna tromboza korionske ploče (+, ++, +++), vaskularna pareza (+, ++, +++).
Hronična insuficijencija (ne, +); - kompenzirano (umjereno izražene involutivno-distrofične promjene i kompenzatorno-prilagodljivi procesi), subkompenzirano(slabe involutivno-distrofične promjene, fokalni ili difuzni poremećaji sazrijevanja vilusa, zadebljanje SCM); dekompenzirano (izražene involutivno-distrofične promjene - velika količina fibrinoida, pseudoinfarkt, kalcifikacija, skleroza vila, vaskularna redukcija sa blagim kompenzacijskim reakcijama i difuzni poremećaji u sazrijevanju vilica).
DIJAGNOZA:
ŠEMA OPISA PLACENTE NOVOROĐENĆE
UROVNI RESEARCH
1. Ograničeno (mikro 6 kom.)
(Normalna donošena beba - Apgar 8-9, PPK 0,12-0,14).
2 Kompleks A (mikro-10 kus., IFLA, parcijalni test krvi)
(nedonoščad, zaostajanje u razvoju, teška hipoksija).
3. Kompleks B (mikro 15-20 cu., IFLA, kompletna krvna slika)
(Vu, mrtvorođenče)
PUPKANA
Makro:
dužina (cm)
Prečnici (maks, min.)
ELM (g/cm)
Broj plovila (3,2,4).
Vezanost (centralna, paracentralna, marginalna, ljuska)
Krvarenje (lokacija, veličina)
Naboranost (slaba, umjerena, izražena).
Pravi čvorovi (lokalizacija, stepen poremećaja krvotoka).
Lažni čvorovi (lokalizacija, struktura - vaskularna petlja, proširene vene, aneurizma).
Druge promjene (adhezije, lomovi, tumori, itd.).
mikro:
Vaskularna struktura (normalna, patološka - hipoplazija, displazija, edem, infiltracija leukocita).
Punjenje krvi (anemija, umjerena kongestija, hiperemija, tromboza).
Krvarenje (lokalizacija, težina - mala, umjerena, opsežna).
Stepen edema (slab - ELM do 1 g/cm, umjeren - ELM -1,0-1,5 g/cm, izražen> 1,5 g/cm).
Infiltracija leukocita (blaga, umjerena, teška).
Druge promjene (ostaci alantoisa i žumančane vrećice, hipoplazija ili aplazija Whartonovog želea, itd.).
Školjke
Makro:
IPC (M o / M kom).
Bez patoloških promjena (tanak, providan, sjajan)
Fibrinoidni plakovi (pojedinačni, višestruki)
Krvarenje, krvni ugrušci.
Patološke promjene - (edematozni, zamućeni, mutni, obojeni).
mikro:
Amnijalna membrana- edem (ozbiljnost), adhezija (fokalna, difuzna), infiltracija leukocita.
Trofoblastni sloj - bistroćelijski, tamnoćelijski, ujednačeni, neravni; hiperplazija, hipoplazija;
citolitičke promjene (fokalne, difuzne),
infiltracija leukocita (fokalna, difuzna), nakupljanje leukocita u submezodermalnoj zoni.
Fibrinoidna zona
odsutan, beznačajan (fokalni), izražen (široko rasprostranjen).
Decidualni sloj kompaktan, spužvast, tanak, izražen,
limfocitna infiltracija (stepen težine, difuzna ili žarišna),
infiltracija leukocita (stepena ozbiljnosti, difuzna ili žarišna),
vaskularno stanje (cirkulacija krvi, vaskulitis),
hemoragije, nekroze (lokalizacija, veličina, struktura, ćelijska reakcija).
PLACENTA
Makro:
Oblik (okrugli, ovalni, nepravilni)
Prečnik (veliki, mali)
Debljina (rez)
Masa (bez omotača i pupčane vrpce)
Anomalije razvoja (jastuk, rub, akcesorni režanj, itd.)
Horionska ploča:
Amnijalna membrana je tanka, sjajna; nema patoloških promjena; krvni ugrušci, krvarenja.
Bazalna ploča:
Reljef (zaglađen, kvrgav); nema patoloških promjena;
kalcifikacija (ozbiljnost);
praznine, nedostaci (veličina, količina, lokalizacija);
krvarenja, koagulacija krvi (veličina, lokalizacija, adhezije)
placentno tkivo - konzistencija (gusta, spužvasta, mlohava), boja (cijanotična, tamnocijanotična, blijedocijanotična), bez patoloških promjena;
krvni ugrušci, srčani udari (lokalizacija, veličina, boja)
mikro:
korionske resice - stepen razvoja TBH (normalan, hipoplazija, hiperplazija, displazija);
vaskularizacija TBX (normalna, smanjena, povećana);
TBX punjenja krvi (anemija, umjerena ili teška pletora), dijapedetske hemoragije;
manifestacije hematogene infekcije (viluzitis, interiluzitis);
Krvno punjenje interviloznog prostora (anemija, umjerena, izražena);
Krvni ugrušci, srčani udari (struktura, stepen organizacije).
Involutivne promene - fibrinoidne naslage, kalcifikacija, fibroza (težina - umerena, izražena: prevalencija - ograničena marginalna, difuzna).
bazalna ploča - bez patoloških promjena.
Fibrinoidni slojevi (ujednačeni, neravni, tanki, zadebljani, bezoblični).
Decidua (tanka, zadebljana; kompaktna, spužvasta), ćelijska infiltracija (sastav, težina), nekroza (struktura, veličina, ćelijski odgovor), hemoragije (struktura, veličina, ćelijski odgovor).
OPCIJE ZAKLJUČKA
Normalno održivo novorođenče (1. nivo)
Normoplastični tip strukture posteljice. Reaktivne promjene u posteljici.
Kompenzatorna hiperplazija placente. Reaktivne promjene u posteljici.
Opcije su: transekcija pulsirajuće pupčane vrpce. Taloženje fetalne krvi u porođaju (sa CS), rizik od anemije.
Novorođenčad u riziku (2. nivo)
3. Hronična placentna insuficijencija:
Oblik: hiperplastični, hipoplastični, displastični, angiospastični.
Stadij: kompenzirana (TBX pletora), subkompenzirana (TBX anemija).
Faktori rizika- placentna kardiopatija (kompenzovano hronično zatajenje bubrega). Kardiopatija placente, anemija (subkompenzirana hronična bubrežna insuficijencija). Prolazna hiperglikemija, metabolički poremećaji (displastični oblik kroničnog zatajenja bubrega).
4. Akutna placentna insuficijencija:
Oblici - paretični (placentalni šok), ishemijski (kardiogeni šok).
Faktori rizika- hipoksična kardiopatija, encefalopatija.
5. Ascendentna bakterijska infekcija placente (stadij). Eksudativna upala membrana (horiodeciduitis, membranitis), placente (subhorijski interluzitis, horioamnionitis), pupčane vrpce (varijeteti funikulitisa)
Faktori rizika -
Za majku - UGI, endocervicitis, endometritis.
Za fetus - amnijalna pneumonija, sepsa (uzimajući u obzir održivost)
Opcija- minimalne manifestacije uzlazne bakterijske infekcije placente (fokalni horodeciduitis), reakcija na normalnu mikrofloru.
6. Hematogene infekcije placente s oštećenjem membrana (fokalni eksudativno-nekrotični deciduitis), placente (produktivni hipertrofični vilusitis, bazalni produktivni deciduitis), pupčane vrpce (trombvaskulitis, eksudativno-nekrotični funiculitis).
7. Hronična insuficijencija pupčane vrpce zbog vaskularne displazije (aplazija arterija, displazija proširenih vena, kombinovana arteriovenska displazija).
Oblici - kompenzirani, subkompenzirani (hronični edem pupčane vrpce).
Faktori rizika- sistemska vaskularna patologija VIRS-a.
Morfološki kriterijumi za akutnu i hroničnu placentnu insuficijenciju (Milovanov).
Karakteristike retrohorijalnog hematoma.
Tokom prvog tromjesečja, najkarakterističniji oblik embriohorijalne insuficijencije je formiranje retrohorijalnog hematoma, koji uzrokuje smrt embrija. Njegova patogeneza određena je nesavršenošću hemostaze u ovom periodu razvoja placente, posebno četkice sincitiotrofoblasta. Placentalna alkalna fosfataza (PLAP) je jasan imunomorfološki marker ruba četkice. Zaostajanje u njegovom razvoju često se opaža u resicama koje graniče s retrohorijalnim hematomom.
Klasifikacija placentne insuficijencije.
A. Blastopatije i patologije implantacije, uključujući komplikacije višeplodnih trudnoća, abnormalnosti u obliku posteljice i vezivanja pupčane vrpce.
B. Patologija ekstraembrionalnih struktura i početna histogeneza embrija.
C. Patologija placente i početna organogeneza embrija.
D. Patologija placente i kasna organogeneza, uključujući spontane pobačaje i "smrznute" trudnoće.
II. Insuficijencija placente koja se razvija u II i III trimestru:
E. Akutni oblici:
1) Akutni poremećaji uteroplacentalne cirkulacije.
2) Akutni poremećaji placentno-fetalne cirkulacije.
E. Hronična placentna insuficijencija:
1) Uteroplacentarni oblik.
2) Placentarni oblik.
3) Placentalno-fetalni oblik.
I stepen - minimalne promjene.
II stepen - promjene umjerene težine
III stepen - teške promene
IV stepen - u slučaju smrti.
Poglavlje 10FETOPLACEENTALNA INSUFICIJENCIJA
Poremećaji morfofunkcionalnog stanja posteljice jedan su od glavnih razloga komplikovanog tijeka trudnoće i porođaja, kao i perinatalnog morbiditeta i mortaliteta.
Patološke promjene koje se javljaju s placentnom insuficijencijom (FPI) dovode do:
Smanjenje uteroplacentarnog i fetoplacentarnog krvotoka;
Smanjena opskrba arterijskom krvlju placente i fetusa;
Ograničenje izmjene plinova i metabolizma u fetoplacentarnom kompleksu;
Kršenje procesa sazrijevanja placente;
Smanjenje sinteze i neravnoteža placentnih hormona i njihovih prekursora majčinog i fetalnog porijekla.
Sve ove promjene potiskuju kompenzatorne i adaptivne sposobnosti sistema majka – posteljica – fetus, usporavaju rast i razvoj fetusa, uzrokuju komplikovan tok trudnoće i porođaja (prijetnja preranog prekida trudnoće, preeklampsija, prijevremeni i kasni porođaj, anomalije porođaja, preuranjena abrupcija placente, itd.).
Fetoplacentna insuficijencija je kompleks simptoma u kojem nastaju morfofunkcionalni poremećaji fetusa i placente zbog raznih ekstragenitalnih i ginekoloških bolesti i opstetričkih komplikacija.
Raznolikost opcija za ispoljavanje FPN-a, učestalost i težina komplikacija za trudnicu i fetus, dominantni poremećaj jedne ili druge funkcije placente ovise o trajanju trudnoće, jačini, trajanju i prirodi trudnoće. uticaj štetnih faktora, kao i na fazu razvoja fetusa i posteljice, težinu kompenzacionih i adaptivnih sposobnosti sistema majka - posteljica - fetus.
^ 10.1. Uzroci i faktori rizika
Fetoplacentarna insuficijencija može se razviti pod utjecajem različitih razloga. Poremećaji u formiranju i funkciji posteljice mogu biti uzrokovani bolestima srca i krvožilnog sistema trudnice (srčane mane, zatajenje cirkulacije, arterijska hipertenzija i hipotenzija), patologija bubrega, jetre, pluća, krvi, kronične infekcije , bolesti neuroendokrinog sistema (dijabetes melitus, hipo- i hiperfunkcija štitne žlijezde, patologija hipotalamusa i nadbubrežnih žlijezda) i niz drugih patoloških stanja.
FPN at anemija zbog smanjenja nivoa gvožđa kako u majčinoj krvi tako i u samoj posteljici, što dovodi do inhibicije aktivnosti respiratornih enzima i transporta gvožđa do fetusa.
At dijabetes melitus poremećen je metabolizam, otkrivaju se hormonski poremećaji i promjene u imunološkom statusu. Sklerotična vaskularna bolest dovodi do smanjenja dotoka arterijske krvi u placentu. U pozadini ove patologije, FPI karakterizira odgođeno ili prerano sazrijevanje placente s povećanjem ili smanjenjem njene mase.
Razno zarazne bolesti, posebno akutna ili pogoršana tokom trudnoće. Placenta može biti inficirana bakterijama, virusima, protozoama i drugim infektivnim uzročnicima. Uz specifične upalne promjene u posteljici, bilježe se i nespecifične reakcije, čija priroda ovisi o vremenu i putu infekcije.
Infektivna lezija u prvom tromjesečju često je praćena abortusom. Kasnija infekcija može se ograničiti na lokalne promjene, koje ovise o prirodi patogena i putu njegovog širenja.
Važnu ulogu u formiranju FPI igra patologija materice: endometrioza, hipoplazija miometrija, malformacije materice (sedlasta, dvoroga).
Treba uzeti u obzir faktor rizika za FPI mioma materice. Međutim, rizik od FPI kod trudnica sa fibroidima materice varira. U grupu sa visokim rizikom spadaju prvorotkinje starije od 36 godina sa pretežno intermuskularnim rasporedom velikih miomskih čvorova, posebno kada se posteljica nalazi u predelu tumora. S centripetalnim rastom fibroida, submukoznom i cervikalnom lokalizacijom čvorova, kao i sa pothranjenošću tumora, vjerovatnoća FPN i poremećaja razvoja fetusa približava se 85%.
Grupu sa niskim rizikom od FPN-a čine mlade žene do 30 godina starosti bez teških ekstragenitalnih oboljenja, sa malim miomatoznim čvorovima, pretežno subperitonealno u fundusu i telu materice.
Među komplikacijama trudnoće, najčešće povezanim sa FPI, vodeće mjesto zauzimaju preeklampsija,što je zbog poznatih patogenetskih mehanizama i morfofunkcionalnih promjena u sistemu majka-placenta-fetus, koje se dešavaju u ovoj patologiji. Ozbiljnost FPN-a, odnosno, ovisi o težini i trajanju toka gestoze.
^ Prijetnja prekida trudnoće treba posmatrati i kao uzrok i kao posledicu FP. Zbog različite etiologije FPN-a sa prijetnjom prekida trudnoće, patogeneza ove komplikacije ima različite mogućnosti, a prognoza za fetus ovisi o stupnju razvoja zaštitnih i adaptivnih reakcija.
^ Sa niskom lokacijom ili prezentacijom posteljice smanjena je vaskularizacija subplacentalne zone. Tanji zid donjeg segmenta materice ne pruža potrebne uslove za dovoljnu vaskularizaciju posteljice i njeno normalno funkcionisanje. Relativno često, uz ovu patologiju, dolazi do abrupcije placente, praćeno gubitkom krvi.
^ Višeplodna trudnoća predstavlja prirodni FPF model kao rezultat neadekvatnog obezbjeđivanja potreba dva ili više fetusa.
FPN se zasniva na izoserološka inkompatibilnost U krvi majke i fetusa najčešće se javljaju procesi poremećenog sazrijevanja posteljice. Fetus razvija anemiju i hipoksiju, dolazi do kašnjenja u razvoju zbog kršenja procesa sinteze proteina i smanjenja aktivnosti enzima.
Povećanje incidencije komplikacija tokom trudnoće u prisustvu ožiljak na materici određena je brojnim faktorima. Distrofične promjene koje se javljaju u području ožiljka utječu na inervaciju maternice i dovode do patoloških impulsa, što zauzvrat remeti trofizam i pokretljivost prednjeg zida maternice. Trofičke promjene na prednjem zidu maternice često dovode do kršenja uteroplacentalne cirkulacije, posebno kada se posteljica nalazi na prednjem zidu maternice. Ovo takođe objašnjava povećanu učestalost preranog odvajanja placente, kao i vjerovatnoću prijevremenog prekida trudnoće. Lokalizacija posteljice na prednjem zidu maternice naglo pogoršava prognozu trudnoće, kako u pogledu održivosti ožiljka, tako iu pogledu razvoja fetusa.
Funkcionalno stanje posteljice je u velikoj mjeri određeno stepenom njenog razvoja u skladu s gestacijskim periodom i sigurnošću zaštitnih i adaptivnih mehanizama. Usklađivanje zrelosti posteljice sa gestacijskom dobi jedan je od najvažnijih uslova za osiguranje adekvatnog razvoja i zaštite ploda.
Nema sumnje da kasno doba trudnice, opterećena anamneza (abortus, upalne bolesti), loše navike, izloženost nepovoljnim faktorima okoline, loša ishrana, socijalna nesigurnost i nered u domaćinstvu takođe doprinose komplikovanom formiranju posteljice i narušavanje njegove funkcije.
Faktori rizika za razvoj FPI uključuju:
Starost ispod 17 i preko 35 godina;
Nepovoljni društveni uslovi;
Toksični i radijacioni efekti spoljašnje sredine;
Ovisnosti (alkohol, pušenje, droge);
Zarazne bolesti;
Ekstragenitalne bolesti (bolesti kardiovaskularnog sistema, respiratornog sistema, jetre, bubrega, krvi, nervnog sistema, endokrinih organa, imunog sistema);
Ginekološke bolesti (upalne etiologije s poremećenom neuroendokrinom regulacijom menstrualne funkcije, praćene neoplazmama);
Nepovoljna akušerska i ginekološka anamneza (neplodnost, ponovljeni pobačaji, spontani i izazvani pobačaji, prevremeni porod, produžena trudnoća, mrtvorođenost, abdominalne operacije na karličnim organima, ožiljak na maternici, kiretaža zidova materice, komplikovan tok prethodne trudnoće i porođaj);
Komplikacije ove trudnoće (rana toksikoza, višeplodna trudnoća, karlična prezentacija ploda, abnormalna lokacija placente, preeklampsija, izosenzibilizacija krvi majke i fetusa).
Navedeni faktori prvenstveno dovode do poremećaja uteroplacentalne, a potom i fetoplacentalne cirkulacije. Zbog stalnih promjena razvijaju se ireverzibilni morfološki procesi i poremećene su glavne funkcije posteljice.
Klinička praksa i rezultati istraživanja ukazuju multifaktorske prirode FPN. S tim u vezi, gotovo je nemoguće izdvojiti bilo koji faktor u razvoju ove komplikacije. Navedena patološka stanja ne utiču podjednako na razvoj FPN-a. Najčešće je nekoliko etioloških faktora uključeno u razvoj ove patologije, od kojih jedan može biti vodeći.
10.2. Patogeneza
Poznavanje glavnih karika patogeneze FPN je temelj za ispravnu dijagnozu, liječenje i prevenciju ove komplikacije trudnoće.
U razvoju FPN može se razlikovati nekoliko međusobno povezanih patogenetskih faktora:
Nedostatak invazije citotrofoblasta;
Patološke promjene u uteroplacentarnoj cirkulaciji;
Kršenje placentnog krvotoka;
Nezrelost stabla vila;
Smanjenje zaštitnih i adaptivnih reakcija;
Oštećenje placentne barijere.
Morfogeneza placente u velikoj mjeri ovisi o razvoju BMD. Prema podacima morfoloških studija, od 16-18 dana uočava se proces invazije intersticijalnog citotrofoblasta. U 5-6 sedmici invazijski procesi postaju najintenzivniji pojavom intravaskularnih ćelija citotrofoblasta u lumenu endometrijalnih segmenata spiralnih arterija. Prvi talas Invazija citotrofoblasta pospješuje širenje i otvaranje spiralnih arterija u intervillous prostor, što osigurava početak i povećanje BMD. Do kraja 10. tjedna formira se sistem razjapljenih uteroplacentnih arterija sa širokim lumenom i stalnim protokom krvi na cijelom području decidua basalis. Prvi talas invazije citotrofoblasta izumire u roku od 11-14 nedelja.
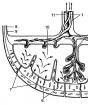
U 16-18 sedmici počinje trudnoća drugi talas invazija citotrofoblasta zbog migracije intravaskularnog citotrofoblasta duboko u zidove miometrijskih segmenata spiralnih arterija, što je praćeno destrukcijom elastomuskularnih komponenti krvnih žila i njihovom zamjenom fibrinoidom (slika 10.1). Istovremeno se opaža prodiranje intersticijalnog citotrofoblasta u miometrij koji aktivira promjene u vaskularnom zidu sa strane adventicijske membrane.
Rice. 10.1. Promjene na spiralnim arterijama tokom invazije citotrofoblasta.
1 - endometrijum; 2 - miometrijum; 3 - miometrijski segment spiralne arterije; 4 - endometrijalni segment spiralne arterije; 5 - protok krvi kroz spiralnu arteriju u intervillous prostor.
Kao rezultat razaranja mišićnih elemenata endo- i miometrijskih segmenata spiralnih arterija, njihov lumen se značajno širi i gubi sposobnost reagiranja na djelovanje vazopresorskih faktora, što osigurava daljnje povećanje BMD.
Pretpostavlja se da decidualne ćelije, koje proizvode lokalno delujuće regulatore proliferacije i invazije citotrofoblasta, imaju kontrolnu ulogu u ovom složenom procesu.
Promjene koje se dešavaju na zidovima spiralnih arterija treba smatrati adaptivnim fiziološkim procesom koji ima za cilj osiguravanje kontinuiranog adekvatnog dotoka krvi u intervillousni prostor.
Ako se do kraja prvog tromjesečja trudnoće prvi val invazije citotrofoblasta ne realizuje u potpunosti (očuvani su elastomuskularni elementi endometrijalnih segmenata spiralnih arterija), onda to dovodi do značajnog smanjenja volumena dotočne krvi majke. i kašnjenje u početku BMD. U decidua basalis se formiraju zone nekroze koje dovode do odvajanja placente i smrti embrija.
Rezultati brojnih studija posteljice u drugoj polovini trudnoće sa gestozom, hipertenzijom trudnica i zastojem u razvoju fetusa ukazuju da ovim patološkim stanjima često prethodi neuspjeh drugog talasa invazije citotrofoblasta u miometrijske segmente spiralnih arterija. Žile čuvaju endotel, srednju membranu i elastične membrane. Uzak lumen spiralnih arterija, njihova otpornost i osjetljivost na vazomotorne podražaje, ometa normalan protok krvi, ne osigurava adekvatno povećanje BMD-a i dovodi do smanjenja opskrbe placente krvlju i ishemije resica.
Moguće je da se arterijska hipertenzija povezana s trudnoćom razvija kao kompenzacijska reakcija, koja ima za cilj povećanje protoka krvi u intervillousni prostor kao odgovor na insuficijenciju drugog vala invazije citotrofoblasta.
Poremećaj protoka krvi u spiralnim arterijama je također praćen hemoragijskim poremećajima u interviloznom prostoru. Patologija spiralnih arterija može dovesti do preranog odvajanja placente i do njenog akutnog hemoragijskog infarkta.
Jedan od vodećih faktora u patogenezi FPN je kršenje uteroplacentalne cirkulacije, koji se zasniva na morfofunkcionalnim promjenama u vaskularnom sistemu i njegovim pojedinim komponentama, pri čemu se poseban značaj pridaje poremećajima u bazenu spiralnih arterija i u interviloznom prostoru.
Do 10-12. tjedna fiziološke trudnoće završava se period placentacije, koji karakterizira vaskularizacija resica i transformacija sekundarnih resica u tercijarne. Glavna strukturna jedinica posteljice postaje kotiledon, koji se sastoji od resica stabljike s granama koje sadrže žile fetusa. Središnji dio kotiledona čini šupljinu, koja je okružena resicama drugog i trećeg reda. U zreloj posteljici ima od 30 do 50.

Rice. 10.2. Struktura placente i uteroplacentalna cirkulacija.
1 - arterije pupčane vrpce; 2 - resice stabljike; 3 - decidualni septum; 4 - decidualni sloj;
5 - miometrijum; 6 - vene; 7 - spiralne arterije; 8 - horion; 9 - amnion; 10 - međuvilozni prostor;
11 - vena pupčane vrpce.
Intervillozni prostor na strani ploda formiraju korionska ploča i resice koje su pričvršćene za njega, a na majčinoj strani omeđen je bazalnom pločom, deciduom i septama koji se pružaju iz nje (sl. 10.2).
Spiralne arterije, koje su završne grane arterija maternice i jajnika koje hrane matericu, otvaraju se svojim ustima u međuvilozni prostor 120-150. Kao rezultat gestacijskog preuređivanja spiralnih arterija, osigurava se stalan protok krvi majke bogate kisikom u intervillous prostor.
Zbog razlike u tlaku, koja je veća u arterijskom krevetu majke u odnosu na intervillous prostor, oksigenirana krv iz otvora spiralnih arterija usmjerava se kroz centar kotiledona do resica, stiže do korionske ploče i vraća se u krvotok majke kroz venske otvore duž septa koji se razdvajaju.
Gusta mreža terminalnih i srednjih resica čini kapilarnu vezu BMD, gdje se difuzija plinova i razmjena nutrijenata između krvi majke i fetusa odvija kroz placentnu barijeru.
Odliv krvi iz interviloznog prostora odvija se kroz venske otvore, od kojih se većina nalazi u blizini septa koji razdvajaju kotiledone. Venski otvori i manifoldi ne prolaze kroz gestacijsko preuređenje; oni čuvaju endotelnu sluznicu i pojedinačne glatke mišićne ćelije.
Vene posteljice iz gornjeg dijela tijela materice prelaze u aciniformni pleksus, a iz donjeg dijela u sistem vene materice, formirajući brojne anastomoze.
U pozadini očuvanja mišićnih elemenata u zidovima žila subplacentalne zone, potpune ili djelomične opturacije žila zbog aterosklerotskih promjena, poremećaja vaskularno-trombocitne veze, tromboze ili mikroembolije, javljaju se poremećaji u vaskularnom sistemu. materice, intervillous prostora, krvnih sudova posteljice i pupčane vrpce.
Treba uzeti u obzir da je sistem snabdijevanja krvlju materice samo dio općeg krvožilnog sistema ženskog tijela. Na osnovu toga, patologija BMD se može smatrati jednom od regionalnih manifestacija neprilagođenosti majčinog organizma i regulatornih mehanizama kardiovaskularnog sistema (autonomni nervni sistem, renin-angiotenzin, serotonin, bradikininski sistem, kateholamini, prostaglandini, itd.), koji mijenjaju tonus krvnih sudova i reološka svojstva krvi.
Poremećaj protoka krvi u pojedinim žilama ne dovodi uvijek do značajnog smanjenja dotoka krvi u placentu, jer se nadoknađuje kolateralnim protokom krvi. Ako je kolateralna cirkulacija nedovoljno izražena, dolazi do poremećaja mikrocirkulacije, ishemije i degeneracije placente.
Kršenje IPC-a karakteriziraju sljedeći najvažniji faktori:
Smanjen dotok u intervillozni prostor;
Poteškoće u odlivu iz interviloznog prostora;
Promjene u reološkim i koagulacijskim svojstvima krvi majke i fetusa;
Poremećaj kapilarnog protoka krvi u horionskim resicama.
Daleko najvažniji, ali ne i jedini razlog smanjenje dotoka krvi u intervillozni prostor je odsustvo gestacijskog preuređivanja miometrijskih segmenata spiralnih arterija kao rezultat insuficijencije drugog vala invazije citotrofoblasta.
Određenu ulogu u smanjenju intenziteta krvotoka u uteroplacentarnim žilama imaju hipovolemija (koja se javlja kod trudnica s gestozom), arterijska hipotenzija ili niska lokalizacija posteljice (donji segment, placenta previa).
Srčane mane kod trudnica i smanjenje kontraktilne aktivnosti miokarda također dovode do smanjenja dotoka krvi u maternicu. Anemija trudnica doprinosi smanjenju razmjene plinova i oksigenaciji krvi fetusa.
Smanjenje BMD ima ozbiljan uticaj na formiranje FPI. v zbog činjenice da je nivo izmjene plinova u većoj mjeri rezultat brzine protoka krvi nego difuzijskih svojstava posteljice. Posljedično, usporavanje protoka krvi u spiralnim arterijama i međuviloznom prostoru uvijek dovodi do smanjenja razmjene plinova između krvi majke i fetusa.
Kršenje odljeva krvi iz interviloznog prostora bilježi se kod kardiovaskularnih i plućnih bolesti, sa hipertonusom i povećanom kontraktilnom aktivnošću materice. Tokom kontrakcija materice, pritisak u miometrijumu, amnionskoj šupljini i u interviloznom prostoru značajno raste. U ovom slučaju, krvni tlak u uteroplacentarnim arterijama se ne mijenja značajno, a venski odljev praktički prestaje. Na toj pozadini dolazi do daljnjeg povećanja tlaka i značajnog usporavanja cirkulacije krvi u međuviloznom prostoru. Naknadno povećanje pritiska u interviloznom prostoru do nivoa koji prelazi sistemski arterijski pritisak služi kao prepreka protoku krvi kroz spiralne arterije (ishemija placente).
Dakle, kršenje odljeva i protoka krvi uzrokuje nagli pad hemocirkulacije u međuviloznom prostoru i smanjenje razmjene plinova između krvi majke i fetusa.
Smanjenje brzine protoka krvi u interviloznom prostoru, posebno u kombinaciji s narušavanjem sinteze i ravnoteže prostaglandina E 2 i F 2 α, prostaciklina i tromboksana A 2, dovodi do stvaranja tromba, hiperkoagulacije, povećanja viskoziteta krvi, taloženja fibrina , smanjena mikrocirkulacija i razvoj nodularne ishemije.
Bitna uloga u razvoju FP je dodijeljena kršenje placentnog krvotoka. Arterijski sistem FPK, koji prenosi vensku krv od fetusa do placente, predstavljen je sa dvije arterije pupčane vrpce, koje potiču iz zajedničkih ilijačnih arterija fetusa. Završne grane umbilikalnih arterija su arterije i arteriole resica I, II i III reda. Zid pupčane arterije uključuje dva mišićna sloja: - vanjski sa kružnim rasporedom mišićnih snopova i unutrašnji sa njihovim uzdužnim smjerom.
Nastavak arteriola su brojne uvijene kapilare u terminalnim resicama. Na vrhovima terminalnih resica kapilare se šire, formirajući sinusoide, koji se nalaze ispod istanjenog sincitiotrofoblasta i formiraju placentnu barijeru.
Iz kapilarnih petlji na nivou srednje diferenciranih resica polazi venska veza FPK. Dalje od baza potpornih resica, venske žile (nose oksigenisanu krv) usmjeravaju se u debljinu horionske ploče i spajaju se u jednu venu pupčane vrpce, koja je moćna žila elasto-mišićnog tipa, koja prelazi u venski kanal u predjelu fetalne jetre.
Protok krvi u pupčanu vrpcu i posteljicu odvija se zbog kontraktilne aktivnosti fetalnog srca, koje ima ograničen kapacitet za povećanje minutnog volumena. Važan faktor u protoku krvi je prisustvo glatkih mišićnih slojeva u zidovima pupčanih arterija, koji igraju ulogu „dodatnog“ ili „perifernog srca“.
Jedan od mehanizama povratka krvi iz placente u fetus je gravitaciona razlika u položaju posteljice i fetusa (posteljica je viša ili na istom nivou sa srcem fetusa), što pospješuje otjecanje krvi. kroz pupčanu vrpcu.
Osim toga, ritmičko pulsiranje arterija pupčane vrpce, koje prepliće venu, prenosi se na njene zidove kroz elastični vartonski žele, koji također potiče otjecanje krvi. Vena pupčane vrpce ima svoju kontraktilnu sposobnost, budući da struktura njene mišićne membrane i unutrašnje elastične membrane podsjeća na strukturu elastomišićnih arterija kod odrasle osobe.
Autonomnu regulaciju FPK obezbjeđuje vazodilatatorni i vazokonstriktorski učinak lokalnih humoralnih faktora proizvedenih u placenti ili u fetusu. Vazodilatacijski učinak imaju prostaciklin i endotelni natriuretski peptid, koje proizvode endotelne stanice. Ulogu vazokonstriktora imaju tromboksan A2, angiotenzin II i endotel I.
Uz dominantno kršenje FPK, dolazi do smanjenja cirkulacije krvi u arterijama pupčane vrpce, korionske ploče i potpornih resica, što je popraćeno slikom obliterativne angiopatije. Većina opservacija otkrila je normalne gestacijske promjene u spiralnim arterijama. U više od polovine posmatranja postoji patološka nezrelost resica. Kao rezultat utjecaja lokalnih vazokonstriktornih faktora, uočava se suženje lumena umbilikalnih arterija. Razvija se obliteracija arterija i arteriola u potpornim resicama i smanjuje se kapilarni protok krvi. Kao rezultat hipoksije i aktivacije viloznog citotrofoblasta, distalno smještene resice su potpuno zazidane fibrinoidom, što je posljedica primarnog prestanka cirkulacije krvi u njihovim kapilarama. Isključivanje resica zazidanih fibrinoidom iz interviloznog krvotoka dovodi do poremećaja razmjene plinova, disfunkcije placente i razvoja FPN-a.
Jedan od važnih uzroka disfunkcije placente i razvoja FPN-a je nezrelost stabla vila, što se manifestuje promjenama u svim njegovim strukturnim jedinicama.
Postoji nekoliko varijanti patološke i relativne nezrelosti posteljice.
▲ ^ Varijanta nezrele mezenhimske resice je najraniji oblik nezrelosti posteljice, koji nastaje kao rezultat antenatalnog oštećenja u fazi sekundarnih ili mezenhimalnih resica. Zaustavljanje razvoja vila karakterizira izostanak daljnje diferencijacije mezenhima u pravcu autohtone angiogeneze i drugih komponenti strome.
▲ ^ Varijanta embrionalnih resica zbog perzistiranja resica koje se povlače. Rana patološka nezrelost nastaje kao rezultat antenatalne povrede u intervalu od 21-22 dana do 7-8 nedelja.
Istovremeno, arteriole i venule se ne formiraju u resicama iz kapilara, što može biti uzrokovano neskladom između početka angiogeneze u resicama i brzine formiranja embrionalnog cirkulacionog sistema ili fuzije krvnih žila. pupčana vrpca u razvoju sa stablom vila. Negativan učinak može se pojaviti i zbog neuspjeha prvog vala invazije citotrofoblasta, koji se odvija u isto vrijeme.
Posteljica sadrži 50-60% embrionalnih resica sa ranom toksikozom, izoserološkom nekompatibilnošću krvi majke i fetusa, dijabetes melitusom, infekcijama (toksoplazmoza, rubeola, sifilis).
▲ ^ Varijanta srednjih nezrelih resica karakterizira činjenica da kod antenatalnog oštećenja u intervalu od 8-9 do 16-18 tjedana postoji perzistencija srednje nezrelih resica, koje zadržavaju svoju morfofunkcionalnu aktivnost. Glavni patogenetski mehanizam ove varijante nezrelosti placente je insuficijencija drugog vala invazije citotrofoblasta u miometrijske segmente spiralnih arterija. Odsustvo daljeg rasta volumena BMD-a dovodi do činjenice da stablo vilice do sredine trudnoće nije u stanju da adekvatno realizuje svoje difuzijske sposobnosti.
Varijanta srednje nezrelih resica nalazi se kod rane antenatalne infekcije, dijabetes melitusa, nefritisa i druge somatske patologije u trudnice.
▲ ^ Varijanta srednje diferenciranih resica manifestuje se perzistencijom stabla vila bez formiranja terminalnih resica kao rezultat antenatalnog oštećenja u 21-32 sedmici, kada se normalno javlja intenzivan rast međugrana. Morfološke karakteristike strukture srednje diferenciranih resica dovode do smanjenja površine difuzije viloznog stabla, područja sincitiotrofoblasta koji stvara hormon i volumena međuviloznog prostora. Najčešće, na ovoj pozadini, primjećuje se IUGR fetusa.
▲ ^ Varijanta haotičnih skleroziranih resica nastaje kao rezultat antenatalnih ozljeda u 25-30. tjednu i karakterizira ga kršenje formiranja malih resica s prevlašću stromalne komponente, zaostajanje u razvoju kapilarnog korita i epitelnog pokrivača. Uočeno je poremećeno grananje malih resica sa pojedinačnim uskim kapilarama, koje po svojoj strukturi ne odgovaraju tipičnim terminalnim granama.
Varijanta haotičnih skleroziranih resica često se nalazi kod teške preeklampsije, arterijske hipertenzije i višeplodnih trudnoća.
Navedene varijante patološke nezrelosti posteljice najčešće dovode do smrti fetusa ili do zastoja u njegovom intrauterinom razvoju.
Postoje i dva oblika relativne nezrelosti posteljice.
▲ ^ Prerano sazrijevanje posteljice zbog pojave pretežnog broja tipičnih terminalnih resica prije 32-33 sedmice. Većina ovih resica ne odgovara specijalizovanom tipu terminalnih resica koje se formiraju tokom poslednjeg meseca trudnoće.
▲ ^ Disocirani razvoj kotiledona karakterizira prisustvo zona srednje diferenciranih ili nezrelih resica, kao i odvojene grupe embrionalnih resica, uz prevlast normalnih terminalnih resica koje odgovaraju gestacijskoj dobi.
Neravnomjerno sazrijevanje kotiledona često se opaža kod gestoze. Shodno tome, priroda procesa sazrijevanja placente usko je povezana s različitim opstetričkim patologijama.
U patogenezi FPN značajnu ulogu imaju smanjenje aktivnosti zaštitno-prilagodljivih reakcija u sistemu majka - posteljica - fetus kao odgovor na patološki proces.
Uz fiziološki tekuću trudnoću, ove reakcije imaju za cilj optimalno održavanje funkcije fetoplacentarnog kompleksa. Ozbiljnost FPN-a je u velikoj mjeri određena očuvanjem zaštitno-prilagodljivih reakcija i normalnom strukturom placente.
Normalna razmjena plinova između tijela majke i fetusa je osigurana adekvatnim stanjem BMD i FPK.
Primjer kompenzacijske reakcije od strane majčinog organizma je povećanje minutnog volumena srca i BCC-a, kao i smanjenje vaskularnog otpora u arterijama maternice.
Čak i uz normalnu trudnoću, količina kisika koja se isporučuje fetusu je manja nego kod odrasle osobe. Ovaj deficit se uspješno nadoknađuje različitim adaptivnim mehanizmima, čime se osigurava normalan razvoj fetusa.
Jedan od ovih adaptivnih mehanizama je visok minutni volumen kod fetusa (3-4 puta veći nego kod odrasle osobe na 1 kg tjelesne težine). Nivo hemoglobina u krvi majke je oko 120 g/l, au krvi fetusa oko 150 g/l. Svaki gram hemoglobina se kombinuje sa 1,34 ml kiseonika. Takvo povećanje sposobnosti krvi da prenosi kisik, zajedno s povećanjem afiniteta krvi fetusa prema kisiku, pomaže da se optimizira njegov prijenos iz krvotoka majke u fetus. Prisutnost anatomskih fetalnih šantova (ductus venosus, ductus arteriosus, foramen ovale) doprinosi činjenici da gotovo svi organi fetusa primaju miješanu krv. U ovom slučaju, pad parcijalnog pritiska kiseonika tokom hipoksije se dešava sporije.
Kompenzacijske reakcije koje osiguravaju otpornost fetusa na hipoksiju uključuju i nizak nivo njegovog metabolizma i visoku aktivnost glikolize.
Kompenzacijske reakcije iz placente manifestiraju se širenjem lumena fetalnih žila. Povećanjem broja terminalnih resica povećava se ukupna izmjenjivačka površina placente kako bi se osigurala dovoljna zasićenost krvi fetusa kisikom.
Najvažniji kompenzacijski mehanizam u drugoj polovini trudnoće je formiranje sincitiokapilarnih membrana, kroz koje se odvija izmjena plinova i transport nutrijenata.
Uz nedovoljnu izmjenu plinova kao kompenzatornu reakciju, povećava se aktivnost anaerobnih metaboličkih procesa, usmjerenih na normalizaciju poremećaja izmjene kisika između majke i fetusa, a smanjuje se potrošnja kisika placente i fetalnog tkiva.
Optimizacija BMD-a je osigurana formiranjem miometrijskih i placentnih arteriovenskih šantova.
Pod uticajem štetnih etioloških faktora koji doprinose nastanku FPN-a, navedene kompenzatorne reakcije mogu biti defektne. Rezerva manifestacije zaštitno-prilagodljivih reakcija ima određenu granicu, nakon čega se javljaju ireverzibilne patološke promjene u fetoplacentarnom kompleksu, što dovodi do dekompenziranog oblika FPN-a, uključujući smrt fetusa.
Oštećenje placentne barijere pod uticajem patoloških faktora se takođe navodi kao jedan od patogenetskih mehanizama razvoja FPN.
Placentarna barijera, koja se sastoji od epitelnog omotača resica, zajedničkog bazalnog sloja sincititrofoblasta i endotelne ćelije susedne kapilare, kao i citoplazmatskog sloja endotelne ćelije, vrši funkcionalnu interakciju između BMD i FPK ( Slika 10.3). Struktura placentne barijere omogućava intenzivnu izmjenu plinova i transport hranjivih tvari između krvotoka majke i fetusa.
Postoji nekoliko načina transporta tvari kroz placentnu barijeru.
▲ Difuzija osigurava kretanje plinova, lipida, vitamina topivih u mastima i nekih lijekova kroz membrane iz područja njihove visoke koncentracije u područje niže koncentracije zbog kretanja molekula.
▲ ^ Olakšana difuzija vrši transport ugljikohidrata i aminokiselina. Posebne molekule nosača hvataju ove tvari iz krvne plazme majke (područje visoke koncentracije) i prenose ih preko placentne barijere u fetalni krvotok (područje niske koncentracije).
▲ ^ Aktivan transport omogućava prijenos tvari u smjeru suprotnom od gradijenta koncentracije. Ovaj vid transporta ostvaruje se uz utrošak energije, jer ovako transportovani aminokiseline, proteini, vitamini i mikroelementi (kalcijum, gvožđe itd.) prethodno podležu određenim hemijskim reakcijama u citoplazmi sincitiotrofoblasta i endotelnih ćelija i transportuju se preko placentnu barijeru uz pomoć molekula nosača.
▲ Pinocitoza podstiče kretanje proteina plazme, imunoglobulina i hormona kroz placentnu barijeru. Mehanizam pinocitoze je da nastale membranske invaginacije hvataju transportirane supstance i transformišu se u vezikule koje se kreću kroz sve slojeve placentne barijere i otvaraju se na njenoj suprotnoj strani.
▲ ^ Defekti placentne membrane omogućavaju krvnim ćelijama majke i fetusa da se kreću kroz placentnu barijeru, kao i patogenima nekih infekcija.

Rice. 10.3. Struktura placentne barijere.
1 - endotel kapilara terminalnih resica; 2 - kapilara resica; 3 - sincitiotrofoblast; 4 - epitelni pokrov resica.
▲ ^ Volumetrijski transport tvari izvedeno pomoću hidrostatskog ili osmotskog gradijenta. Na taj način se transportuju voda i otopljeni elektroliti.
Na regulaciju permeabilnosti placentne barijere utiču brojni enzimi. Propustljivost ćelijskih membrana je takođe posledica ravnoteže između lipidne peroksidacije (LPO) i antioksidativnog odbrambenog sistema u telu majke i fetusa. S razvojem FPN-a, kao rezultat poremećenog metabolizma ugljikohidrata i lipida, LPO se povećava na pozadini smanjenja antioksidativne aktivnosti, što je jedan od važnih uzroka oštećenja staničnih membrana posteljice i narušavanja njihove propusnosti. .
Kao rezultat djelovanja štetnih faktora u I-II trimestru, razvoj FPN-a može biti posljedica dominantne lezije placentne barijere.
Istovremeno se primjećuju i najteže varijante nezrelosti vila s progresivnom stromalnom sklerozom. Dolazi do značajnog smanjenja protoka krvi u kapilarnom krevetu posteljice (kršenje FPC) uz relativno očuvanje BMD, što dovodi do razvoja lokalne hipoksije. Više od polovine opservacija pokazalo je normalno gestacijsko preuređenje spiralnih arterija. Karakterističan histološki znak ove varijante razvoja FPN-a je atrofija sincititrofoblasta i izraženo zadebljanje placentne barijere, što dovodi do kršenja njegove transportne funkcije.
Vodeća uloga određenih patogenetskih mehanizama u nastanku FPN-a je u velikoj mjeri posljedica njegovih etioloških faktora.
Kod gestoze i hipertenzije dolazi do izražaja promjena BMD-a i mikrocirkulacije. Imunološki konflikt se u početku manifestuje narušavanjem permeabilnosti ćelijskih membrana, a cirkulacijski i drugi poremećaji se razvijaju tek sekundarno.
U trudnoći komplikovanoj hormonskim poremećajima, primarna karika u FPI je smanjenje korionske vaskularizacije.
Kao rezultat izloženosti štetnim faktorima i implementacije patogenetskih mehanizama koji dovode do FPN-a, prirodno se razvija. fetalna hipoksija.
Najčešće se (prema mehanizmu razvoja) opažaju arterijsko-hipoksemični i mješoviti oblici hipoksije zbog smanjenja sadržaja kisika u krvi majke, smanjenja BMD-a, kršenja transportne funkcije placentne barijere, promjena reoloških svojstava krvi, anemija, anomalije u razvoju fetusa, kao i niz drugih razloga.
U početnim fazama razvoja hipoksije u fetusa aktiviraju se vazopresorni faktori, povećava se tonus perifernih žila, primjećuje se tahikardija, povećava se učestalost respiratornih pokreta, povećava se motorna aktivnost i povećava minutni volumen srca.
Daljnje napredovanje hipoksije dovodi do promjene od tahikardije do bradikardije, pojavljuje se aritmija, a minutni volumen srca se smanjuje. Adaptivni odgovor na hipoksiju je preraspodjela krvi u korist mozga, srca i nadbubrežnih žlijezda uz istovremeno smanjenje opskrbe krvlju drugim organima. Paralelno, motorna i respiratorna aktivnost fetusa je inhibirana. Zbog prekomjernog nakupljanja ugljičnog dioksida u tijelu fetusa i razvoja metaboličkih poremećaja u fetusu, primjećuju se sljedeće:
Patološka acidoza;
hiperglikemija;
Smanjenje oksidativne i plastične uloge glukoze;
Pražnjenje zaliha glikogena i lipida;
Nedostatak energije;
Kršenje mehanizama hormonske regulacije;
Neravnoteža elektrolita;
Odgođen razvoj.
Priroda i težina oštećenja organa i tkiva fetusa zavise od trajanja i težine hipoksije, kao i od efikasnosti provođenja njegovih zaštitnih i adaptivnih reakcija.
Nezrele resice su obično velike i imaju male, neproširene žile, relativno veliku količinu strome i odsustvo SU. Mogu biti prisutni u zrelim posteljicama kao mala izolirana otočića, koja se nalaze u 97% zrelih posteljica i nisu patološka. Prisustvo takvih resica ukazuje da se rast resica nastavlja u zreloj posteljici. Druga vrsta nezrelosti je kašnjenje u sazrevanju resica, tj. resice u pogledu zrelosti značajno zaostaju za datom gestacijskom dobi. Kašnjenje u sazrijevanju resica uočava se kod dijabetes melitusa, Rh-konflikta, sifilisa, toksoplazmoze, hromozomskih abnormalnosti, posebno kod Downovog sindroma.
Ubrzano sazrijevanje. Karakterizira ga dominacija zrelih resica u prijevremenim placentama. Uočava se kod preeklampsije, hipertenzije, ponavljajućih pobačaja itd. Kombinira se s visokim rizikom od fetalne asfiksije i IUGR.
Sve opisane promjene na resicama mogu se podijeliti u tri grupe ovisno o patogenezi:
- zbog smanjenja uteroplacentarnog krvotoka (preeklampsija ili hipertenzija) - CTF hiperplazija i zadebljanje TFB M;
- zbog smanjenja fetalnog krvotoka - povećanje količine SU i stromalne fibroze;
- neutvrđenog porijekla - fibrinoidna nekroza resica, nedostatak SCM i abnormalnosti zrelosti resica.
Mezenhimalna displazija placente (PMD) ili vezikularni drift pseudočestica. Riječ je o rijetkoj patologiji trudnoće, koja makroskopski podsjeća na promjene na posteljici s djelomičnim cističnim zamahom, ali s normalnim kariotipom fetusa. Takvi slučajevi se često pogrešno smatraju djelomičnim stvaranjem plikova. U svjetskoj literaturi je opisan oko 51 slučaj PMD-a.
Makroskopski: posteljica je uvećana, arterije korionske ploče su aneurizmatički proširene, a vene proširene proširene, na površini majke su velika polja cističnih izmijenjenih resica (podsjećaju na grozdove, kao kod cističnog nanosa). Mikroskopski: među normalnim placentnim tkivom otkrivaju se polja koja se sastoje od uvećanih resica stabljike sa cisternastim formacijama, mogu biti horangiomatozne promjene u resicama. Proliferacija trofoblasta i trofoblastne inkluzije, patognomonične za djelomični cistični drift, nisu pronađeni u PMD-u. Osim toga, uz djelomični cistični drift, bilježi se triploidni kariotip i smanjenje razine P-horiogonadotropina u krvi majke. Kod PMD-a se uočavaju različite fetalne patologije - IUGR, anemija, trombocitopenija, prerano rođenje i intrauterina smrt. Komplikacije kod majke povezane s PMD-om su relativno rijetke. PMD je opisan u Wiedemann-Beckwith sindromu.
Tumori placente. Primarni netrofoblastični tumori placente su rijetki. Opisani su horioangiom, horiokarcinom, teratom, hepatocelularni adenom, lejomiom, heterotopije nadbubrežnog i jetrenog tkiva. U placenti se javljaju metastaze malignih tumora od majke (melanoma, karcinoma dojke, želuca, rektuma, pluća, jajnika, pankreasa, kože, rabdomiosarkoma, Ewingovog sarkoma i meduloblastoma) i od fetusa (neuroblastoma, malignog hepatoblastoma). limfom, sarkom, tumori mozga i sakralni teratomi). U većini slučajeva, metastatske tumorske ćelije su lokalizovane u interviloznom prostoru, a kod leukemije može doći do infiltracije vilozne strome. Kod kongenitalnog pigmentnog nevusa fetusa, nevus ćelije se uočavaju u stromi resica i zrnca pigmenta melanina u CG ćelijama. Neki autori smatraju da su rezultat aberantne migracije elemenata neuralnog grebena, a ne metastaza u koštanoj srži.
Transplacentalne metastaze na fetus su mnogo rjeđe nego metastaze na placentu. Od toga se češće opisuju metastaze melanoma i adenokarcinoma pluća. U mnogim slučajevima fetus umire in utero, ali postoje zapažanja spontane regresije tumora.
Horioangiom je najčešći benigni tumor placente. Javlja se u 1% slučajeva u neuzorkovanim posteljicama. Makroskopski: pojedinačni, povremeno višestruki čvorovi, okrugli, ovalni ili u obliku bubrega. Ponekad je tumor tamnocrven, mekan, podsjeća na svježe krvne ugruške, ponekad - bijeli, gust, poput srčanog udara. Lokaliziran u debljini posteljice, često izbočen preko površine ploda. Mikroskopski: ima strukturu mješovitog hemangioma (kapilara, sa kavernoznim područjima). Česta su žarišta nekroze, tromboze i kalcifikacije, ponekad prevladava miksomatozna (angiomiksom) ili fibrozna (angiofibroma) stromalna komponenta. Može se kombinovati sa fetalnim hemangiomom. U većini slučajeva nema klinički značaj. Veliki tumori prečnika preko 5 cm mogu imati ozbiljne posljedice. Za majku - polihidramnij sa ili bez prijevremenog porođaja, prenatalno krvarenje zbog odvajanja ili rupture vaskularne pedikule tumora. Za fetus i novorođenče - hemangiomi u jetri i koži fetusa, kardiomegalija, zatajenje srca, IUGR, vodena bolest, anemija i trombocitopenija, masivno krvarenje placente zbog rupture tumora i fetalne smrti. Posebna varijanta horioangioma je horangiokarcinom, koji ima strukturu horioangioma, ali uz prisustvo proliferirajućih trofoblastnih ćelija. Tumor je benigni, njegove metastaze kod majke ili fetusa nisu opisane.
Horiokarcinom posteljice (choriocarcinoma in situ), koji se makroskopski često ne otkriva, obično se pogrešno smatra srčanim udarom. Mikroskopski: u interviloznom prostoru postoje žarišta proliferirajućih sincitioblasta i citotrofoblasta, koji se šire na obližnje resice. Može doći do invazije u stromu i krvne sudove resica. Posljedice intraplacentalnog horiokarcinoma su različite. U nekim slučajevima majka i fetus nemaju tumor, u drugim se uočavaju metastaze u plućima i majke i fetusa. Opisano je i masivno krvarenje iz placente. Ponekad se tumor u posteljici ne otkrije, uprkos prisutnosti metastaza u fetusu (u nekim slučajevima to je zbog nedovoljnog pregleda posteljice).
Insuficijencija placente. Termin "placentarna insuficijencija" koristi se za označavanje procesa oštećenja (uglavnom redukcije) funkcije posteljice (perfuzija i/ili difuzija). Ni u kliničkim ni u patološkim dijagnozama, ne treba ga koristiti kao specifičnu nozologiju. Patolog je, na osnovu detaljnog morfološkog proučavanja posteljice, u svom zaključku dužan da naznači koji su procesi pretežno poremećeni, te da govori, barem pretpostavlja se, o prognozi za fetus, a eventualno i za naredne trudnoće.
Morfološke manifestacije smanjenja difuzionog kapaciteta posteljice uključuju:
- prevladavanje kašnjenja ili zaustavljanja razvoja vila (nezrelost) s normalnom ili prekomjernom težinom placente;
- umjerena nezrelost resica s hipoplazijom placente;
- horangijaza ili hipovaskularnost vilica;
- SCM deficit;
- hronični vilitis.
Umjereno izraženi poremećaji placentne difuzije nalaze se u 80% zrelih placenti, što je u posljednjim sedmicama trudnoće praćeno fetalnom hipoksijom, a uz dodatne hemodinamske poremećaje prije ili tokom porođaja može doći do akutne asfiksije i smrti ploda.
Smanjenje perfuzijske sposobnosti posteljice nastaje zbog smanjenja protoka krvi u njoj zbog smanjenja interviloznog prostora i/ili fetalnih žila u kombinaciji s hipoplazijom placente, kroničnim poremećajima cirkulacije i/ili poremećenim sazrijevanjem vila.
Glavne morfološke promjene:
- hipoplazija posteljice i generalizirano prerano sazrijevanje resica s nedostatkom srednjih resica;
- hipoplazija posteljice sa raširenim peri- i intraviloznim fibrinoidnim naslagama ili sa srčanim udarima koji zauzimaju više od 30% površine placente;
- obliterirajuća angiopatija sa fibrozom ili nezrelošću resica i izraženim naslagama fibrinoida sa normalnom masom placente za datu gestacijsku dob;
- povećanje broja SU;
- zadebljanje HFBM;
- nedostatak terminalnih resica u zreloj posteljici.
Poremećaji perfuzije imaju štetne posljedice po fetus i novorođenče - intrauterina asfiksija, IUGR, mrtvorođenost, povećan perinatalni morbiditet (posebno hipoksično oštećenje mozga) i mortalitet.